Le esigenze internazionali in materia di sicurezza per i pazienti hanno portato molti paesi ad adottare normative e regolamenti per identificare i “Dispositivi Medici” (lenti a contatto, bende, bisturi, siringhe, protesi dispositivi diagnostici in vitro).
La codifica UDI (Identificativo Univoco del Dispositivo) fornisce tutte le informazioni standardizzate relative al ciclo di vita del dispositivo: dalla sua produzione fino all’utilizzo finale per provarne l’autenticità.
USA (con il regolamento Food and Drug Administration FDA), UE (con i regolamenti Medical Devices Regulation MDR 2017/745 e IVDR 2017/746) hanno approvato dei regolamenti per l’identificazione dei dispositivi medici mentre in Canada, Giappone, Cina, Brasile, Sud Corea, Cina, Israele, Arabia Saudita e Sudafrica sono in via di definizione.
Come serializzare i dispositivi medici con la marcatura e le etichettatrici stampa e applica
I produttori devono effettuare l’etichettatura dispositivi medici con specifici codici denominati Identificativi Univoci dei Dispositivi (UDI, Unique Device Identifier). L’UDI è un codice numerico o alfanumerico univoco composto da due parti:
- Identificativo del Dispositivo (UDI- DI, Device Identifier). Identifica la versione o il modello specifico di un prodotto (obbligatorio e fisso).
- Identificativo della Produzione (UDI- PI, Production Identifier). È variabile e può contenere uno o più delle seguenti informazioni:
- Numero di lotto
- Data di produzione
- Data di scadenza
- Numero di serie
Queste informazioni devono essere fornite sia in un formato leggibile dall’uomo (testo alfanumerico) sia in un formato leggibile dalle macchine che utilizzi la tecnologia AIDC (Automatic Identification and Data Capture).
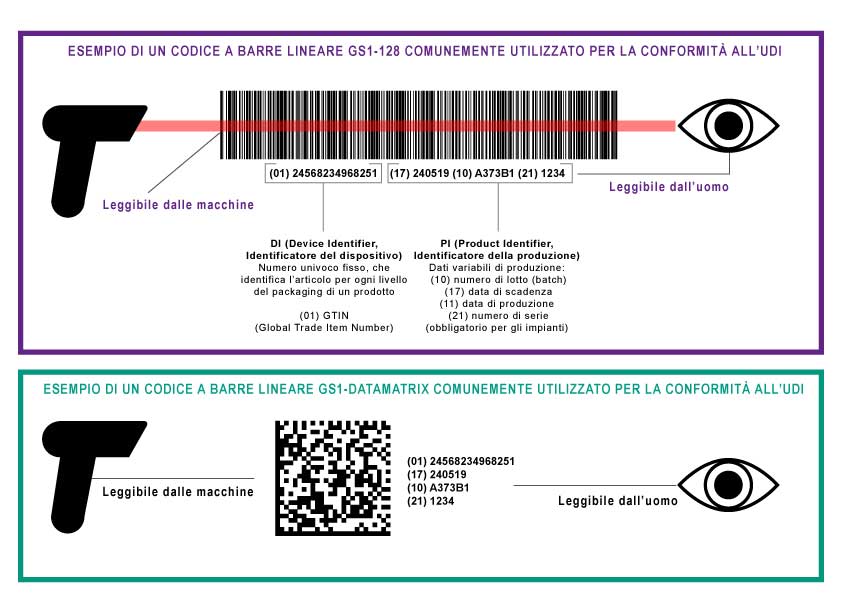
Un codice UDI deve essere posizionato sul packaging primario e a tutti i livelli superiori del packaging del dispositivo. Poiché il GTIN (Global Trade Item Number, un numero identificativo rilasciato da GS1) è univoco per ogni livello del packaging del dispositivo, anche il codice UDI è univoco a qualsiasi livello del packaging.
La marcatura diretta permette infatti un’identificazione costante nel tempo, anche quando un dispositivo non è più accompagnato dall’etichetta o dalla confezione.
La soluzione di stampa e applica e di marcatura per i dispositivi medici

Marcatori Laser (UV, Green, Fiber, MOPA, Co2)
Tecnologia ideale per la marcatura diretta dei dispositivi medici:
– non danneggia il prodotto garantendone l’integrità
– garantisce contenuti di alta qualità senza difetti, permanenti e chiaramente leggibili
– resistenti a processi di pulizia altamente alcalini, acidi, corrosivi.

Etichettatrici stampa e applica
Le etichettatrici stampa e applica rappresentano la tecnologia ideale per stampare un codice UDI in tempo reale su un’etichetta e applicarla su un prodotto, un imballo secondario o un pallet: una soluzione idonea per il processo di aggregazione dei codici (creazione della relazione parent-child tra i codici univoci delle confezioni unitarie ed i codici UDI dei livelli di imballaggio successivi) migliorando la tracciabilità dei dispositivi medici.
CLASSIFICAZIONE DEI DISPOSITIVI MEDICI
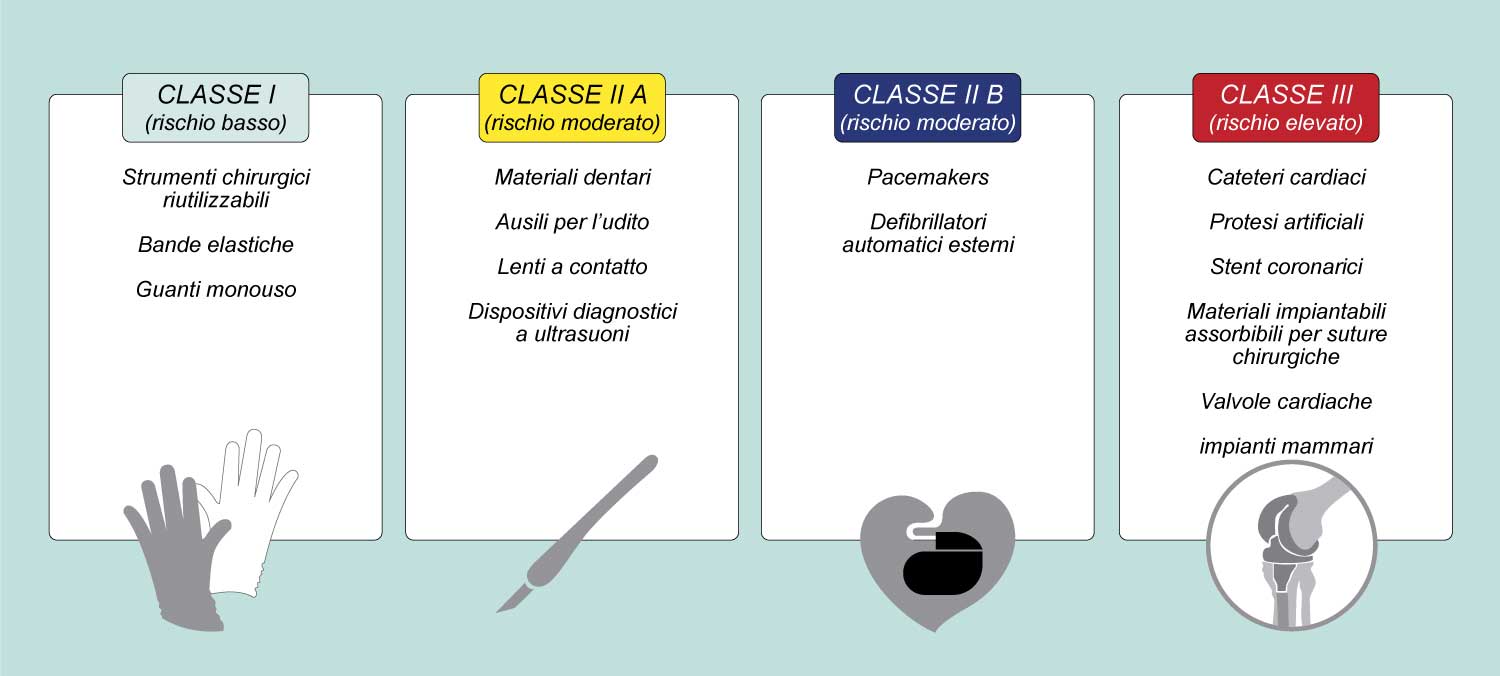
La classificazione del dispositivo medico è basata sul livello di rischio associato al dispositivo in esame.
- Dispositivi di Classe III: cateteri cardiaci, stent coronarici, valvole cardiache, impianti mammari, test diagnostici dell’HIV, impianti endossei, protesi artificiali, lenti a contatto a utilizzo prolungato, materiali impiantabili assorbibili per suture chirurgiche…
- Dispositivi di Classe II b: Pacemaker, defibrillatori automatici esterni, aghi per agopuntura, pompe per infusione…
- Dispositivi di classe II a: Lenti a contatto giornaliere, sedie a rotelle motorizzate, teli chirurgici, materiali dentari, ausili per l’udito, dispositivi diagnostici a ultrasuoni…
- Dispositivi di Classe I: Bende elastiche, guanti in lattice, strumenti chirurgici portatili e riutilizzabili.
Leggi anche l’articolo: Soluzioni Arca per antieffrazione e tracciabilità